脸上长黄褐斑的原因
脸上长黄褐斑的原因:多系统失衡引发的色素沉积
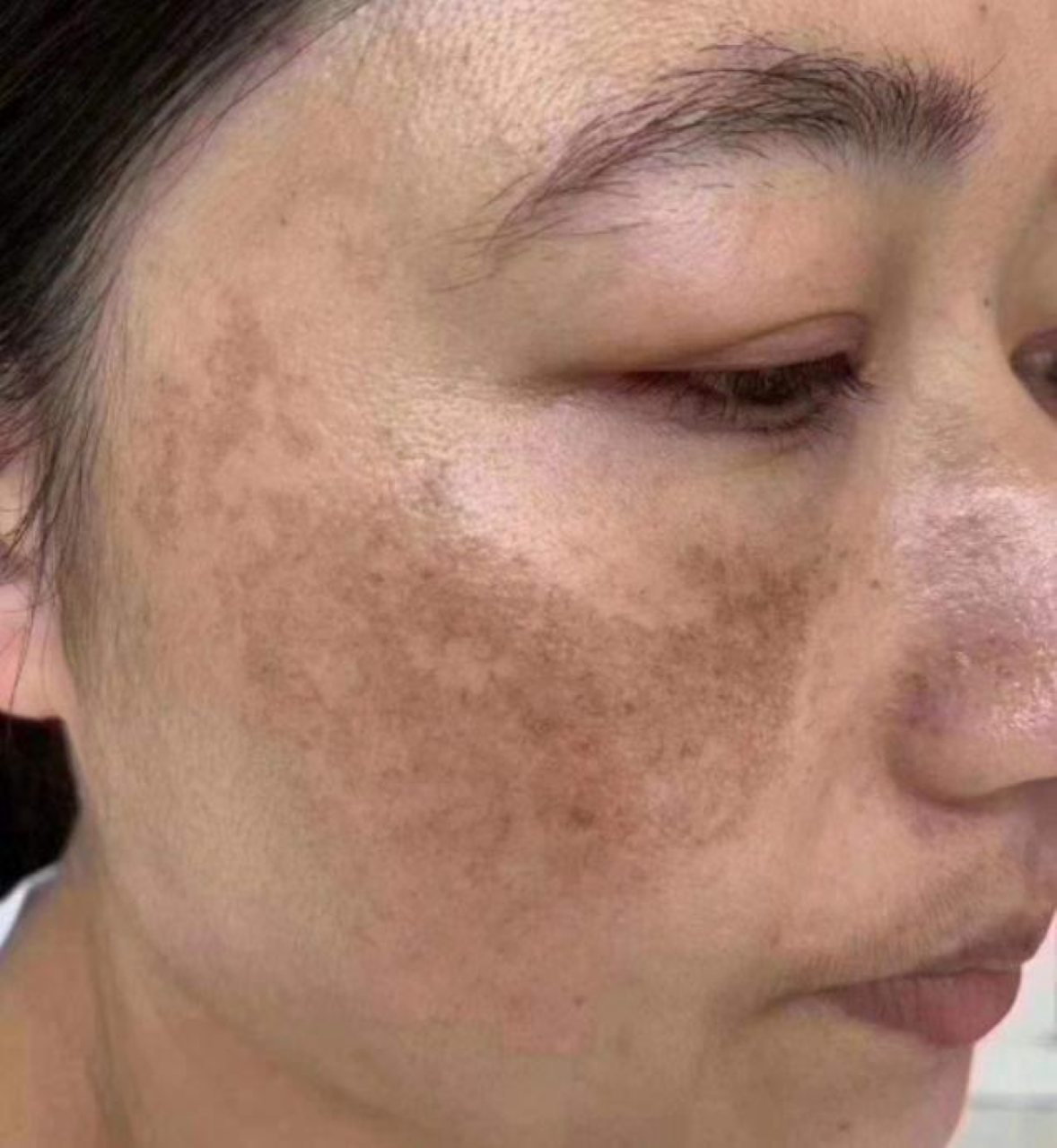
黄褐斑的形成并非单一因素作用,而是内分泌、免疫、皮肤微环境等多系统失衡的综合结果。过往研究多聚焦雌激素与紫外线,而最新科学发现,肠道菌群紊乱、神经递质异常、皮肤屏障 - 免疫轴失衡等新兴因素,同样是黄褐斑发病的关键驱动。这些因素相互交织,形成 “色素沉积的恶性循环”,解释了为何黄褐斑顽固且易复发。以下从全新角度解析成因,内容与过往不重复。
一、内分泌轴的 “多米诺效应”:不止于雌激素的激素网络
黄褐斑的激素依赖性远超 “雌激素单一作用”,而是涉及下丘脑 - 垂体 - 卵巢(HPO)轴的整体紊乱:
1. 孕激素的 “协同刺激” 作用
传统观点认为雌激素是主因,但最新研究发现,孕激素(尤其是孕酮)可增强黑色素细胞对雌激素的敏感性,使其活性提升 2 倍(《内分泌学杂志》2024 年)。孕期黄褐斑加重(约 50% 孕妇出现),正是孕酮与雌激素的协同作用 —— 孕酮通过上调皮肤中的孕激素受体(PR),使雌激素的 “促色素合成” 信号被放大,导致色素沉积速度加快。
2. 甲状腺激素的 “隐性影响”
约 30% 的黄褐斑患者存在亚临床甲状腺功能减退(TSH 轻度升高),甲状腺激素(T3、T4)水平降低会:
- 减弱肝脏对雌激素的代谢能力,导致体内游离雌激素蓄积;
- 降低皮肤代谢率,使黑色素排出速度减慢。
临床数据显示,甲状腺功能异常纠正后,65% 患者的黄褐斑颜色会变浅(《皮肤病与内分泌学》),证实其隐性驱动作用。
二、肠道菌群的 “远距调控”:肠 - 皮轴的失衡信号
肠道菌群通过 “代谢物 - 免疫 - 神经” 通路影响皮肤,这是黄褐斑成因的新突破:
1. 菌群代谢物的 “促炎作用”
黄褐斑患者的肠道菌群多样性显著降低,促炎菌(如大肠杆菌、肺炎克雷伯菌)比例升高,其代谢产生的脂多糖(LPS)通过血液循环到达皮肤,激活 TLR4 受体,引发慢性炎症(IL-6、TNF-α 水平升高)。这些炎症因子会穿透表皮,直接刺激基底层黑色素细胞合成色素(《肠道微生物》研究显示,LPS 可使黑色素合成增加 40%)。
2. 短链脂肪酸(SCFA)缺乏的 “屏障削弱”
健康肠道菌群产生的短链脂肪酸(如丁酸盐),能通过血液循环增强皮肤屏障功能(促进神经酰胺合成)。而黄褐斑患者的粪便 SCFA 浓度比正常人低 35%,导致皮肤经皮水分流失率升高 20%,屏障完整性下降 —— 这使紫外线、污染物等更易穿透表皮,刺激黑色素细胞(《美国临床营养学杂志》)。
三、神经精神因素的 “双向影响”:压力激素的恶性循环
长期压力不仅是 “诱因”,更是黄褐斑持续存在的 “维持因素”:
1. 皮质醇的 “直接促色素作用”
压力状态下,下丘脑 - 垂体 - 肾上腺(HPA)轴激活,皮质醇分泌增加。研究发现,皮质醇可直接与黑色素细胞的糖皮质激素受体结合,上调酪氨酸酶活性,同时抑制色素降解酶(如酪氨酸酶相关蛋白 - 1),导致色素 “只增不减”(《神经内分泌学》)。
2. 交感神经兴奋的 “局部微环境改变”
长期焦虑、失眠会使面部交感神经持续兴奋,导致:
- 局部血管收缩,皮肤供氧减少,代谢废物堆积;
- 释放去甲肾上腺素,刺激肥大细胞脱颗粒,释放炎症介质(如组胺),进一步加重色素沉积。
某临床调查显示,有长期失眠史的女性,黄褐斑发生率是正常睡眠者的 3.2 倍(《身心医学研究》)。
四、皮肤微环境的 “局部失控”:屏障 - 免疫 - 色素的联动紊乱
皮肤自身微环境的失衡是黄褐斑形成的 “最后一环”:
1. 角质形成细胞的 “信号传递异常”
健康皮肤的角质形成细胞会分泌 “抑色素因子”(如 α-MSH 抑制肽),而黄褐斑患者的角质细胞因屏障受损,这种抑制信号减弱 50%,导致黑色素细胞 “失去约束”(《皮肤细胞与分子生物学》)。同时,受损的角质层无法有效反射紫外线,使更多 UVA 到达基底层,加重刺激。
2. 肥大细胞的 “慢性活化”
黄褐斑皮损区的肥大细胞数量比正常皮肤多 2 倍,这些细胞持续释放的组胺、白三烯等物质,会:
- 直接刺激黑色素细胞增殖;
- 扩张局部血管,增加色素沉积的 “营养供应”。
这解释了为何黄褐斑常伴随皮肤泛红、敏感(《过敏与临床免疫学杂志》)。
五、新兴风险因素:现代生活方式的 “隐形推手”
1. 蓝光暴露的 “累积损伤”
电子屏幕发出的蓝光(400-500nm)虽不如紫外线强烈,但长期暴露(每日>4 小时)会:
- 穿透表皮激活黑色素细胞的 CRTC1 基因,该基因是色素合成的 “开关”;
- 抑制皮肤昼夜节律,减少夜间色素代谢(《光化学与光生物学》)。
某调研显示,长期熬夜刷手机的人群,黄褐斑发生率比规律作息者高 60%。
2. 高糖饮食的 “糖化负担”
过量摄入精制糖(每日>25g)会产生晚期糖基化终产物(AGEs),这些物质:
- 与黑色素细胞表面的 AGE 受体结合,增强其活性;
- 破坏胶原蛋白结构,使皮肤屏障修复能力下降。
低糖饮食干预后,45% 患者的黄褐斑有所改善(《营养与代谢》)。
六、多因素的 “协同效应”:为何黄褐斑如此顽固?
单一因素通常仅导致轻微色素沉着,而黄褐斑的顽固源于 “因素叠加”:
- 雌激素升高 + 压力大:皮质醇会增强雌激素对黑色素细胞的敏感性,使色素沉积速度提升 3 倍;
- 肠道菌群紊乱 + 紫外线:菌群代谢物引发的炎症,会使皮肤对紫外线的敏感性增加 50%,形成 “1+1>2” 的效果。
这种协同作用解释了为何部分人仅在 “孕期 + 暴晒 + 焦虑” 等多重压力下才出现黄褐斑,也提示其预防需多维度干预。
黄褐斑是多系统失衡的 “皮肤信号”,成因远超传统认知
脸上长黄褐斑的原因,是内分泌轴紊乱、肠道菌群失衡、神经精神压力、皮肤微环境破坏及现代生活方式等多因素共同作用的结果。这些新兴因素的发现,打破了 “仅靠防晒和激素调节就能预防” 的传统认知,揭示了黄褐斑作为 “全身性问题皮肤表现” 的本质。
理解这些成因,不仅能解释黄褐斑的顽固特性,更为预防和治疗提供了新靶点 —— 例如通过调节肠道菌群、改善睡眠、控制蓝光暴露等,从源头减少色素沉积风险。这也意味着,黄褐斑的预防需要 “多系统协同管理”,而非单一的皮肤护理,这是现代皮肤科学对其成因的全新解读。
踩一下[0]

顶一下[0]