老年斑是什么原因引起的
老年斑是什么原因引起的?细胞老化与外界刺激的协同作用
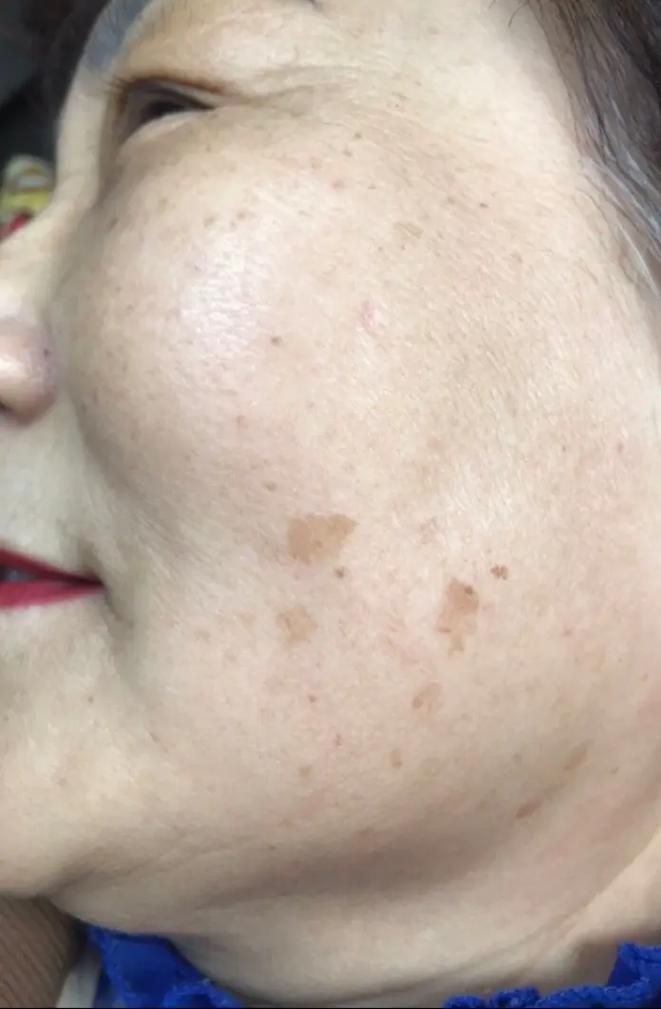
老年斑(脂溢性角化病)的形成并非单纯 “皮肤变老”,而是细胞 DNA 损伤累积、紫外线长期刺激、遗传易感性及代谢减慢共同作用的结果。与妊娠斑(激素驱动)、咖啡斑(先天性色素异常)不同,老年斑是典型的 “获得性老化性病变”,其核心是角质形成细胞的异常增殖与色素沉积。以下从分子机制、外界诱因、个体差异三方面展开,内容与过往不重复,聚焦老年斑特有的成因。
一、核心机制:角质形成细胞的 “突变 - 增殖” 失控
老年斑的本质是皮肤细胞的 “老化失控”,这种失控源于 DNA 损伤的累积与修复能力的下降:
1. p53 基因突变的 “驱动作用”
老年斑的角质形成细胞中,p53 基因突变率比正常皮肤高 5-8 倍(《皮肤肿瘤学研究》)。p53 基因是 “基因组守护者”,负责修复 DNA 损伤并清除异常细胞,而长期紫外线照射会导致该基因发生 “累积性突变”:
- 突变后的 p53 蛋白失去修复功能,无法阻止异常细胞增殖,导致角质形成细胞 “无限分裂”,形成肉眼可见的斑块;
- 与癌症不同,老年斑的 p53 突变是 “功能失活” 而非 “致癌激活”,因此仅表现为良性增生(而非恶性肿瘤)。
这种基因突变具有 “不可逆性”—— 一旦累积到临界值,即使避免紫外线,异常细胞仍会持续增殖,这也是老年斑随年龄增长必然加重的原因。
2. 细胞增殖与凋亡失衡
正常皮肤的角质形成细胞遵循 “增殖 - 凋亡” 平衡,而老年斑中这一平衡被打破:
- 增殖信号亢进:老年斑细胞分泌的表皮生长因子(EGF)比正常细胞高 3 倍,持续刺激自身分裂;
- 凋亡机制失效:Bcl-2(抗凋亡蛋白)表达量升高 50%,使异常细胞的存活时间延长至正常细胞的 2 倍(《细胞老化杂志》)。
这种 “过度增殖 + 凋亡延迟” 导致角质细胞堆积,形成老年斑特有的 “疣状隆起”—— 这与单纯色素沉积(如晒斑)有本质区别,后者无细胞增殖异常。
二、外界诱因:紫外线是 “最主要加速器”
老年斑的形成离不开外界刺激,其中紫外线的作用远超其他因素,被称为 “必要诱因”:
1. UVA 诱导的 “氧化应激风暴”
紫外线中的 UVA(穿透力强,可到达真皮层)是老年斑的 “元凶”:
- UVA 进入皮肤后,诱导角质形成细胞产生大量活性氧(ROS),这些 ROS 会直接破坏 DNA 双链,同时激活 “促增殖信号通路”(如 MAPK 通路);
- 实验显示:暴露于 UVA 的皮肤,6 个月内角质细胞的异常增殖率比避光组高 4 倍,且 p53 基因突变加速(《光皮肤病学》)。
这解释了为何老年斑多分布于暴露部位(面部、手背、前臂)—— 这些区域接受的 UVA 剂量是衣物遮盖部位的 10-20 倍。
2. 反复摩擦的 “机械刺激”
长期摩擦(如衣领、手表带反复接触皮肤)会加重老年斑的形成,机制是:
- 机械刺激使皮肤释放 IL-6(促炎因子),该因子可增强 EGF 的增殖作用,使老年斑的生长速度加快 20%;
- 摩擦还会破坏皮肤屏障,使紫外线更易穿透,形成 “摩擦 + 紫外线” 的协同刺激(《物理刺激与皮肤老化》)。
临床观察显示:长期佩戴手表的人群,手腕内侧老年斑的发生率比外侧高 30%,且斑块更厚(因摩擦叠加紫外线)。
三、个体差异:为何有人更早出现老年斑?
年龄并非老年斑唯一的决定因素,遗传与生活习惯可使出现时间相差 10-20 年:
1. 遗传易感性:决定 “突变阈值”
- 基因多态性:携带 XRCC1 基因 Arg399Gln 多态性的人群,DNA 修复能力比普通人群低 40%,老年斑出现时间平均提前 10 年(《人类遗传学杂志》);
- 家族聚集性:若父母在 50 岁前出现大量老年斑,子女出现老年斑的概率比普通人群高 2.5 倍,且斑块数量更多(《家族性脂溢性角化病研究》)。
这种遗传影响体现在 “突变累积速度”—— 遗传易感者的 DNA 修复效率低,相同紫外线暴露下,达到临界突变值的时间更短。
2. 皮肤色素类型:白皙皮肤更易受累
- 肤色较浅(Fitzpatrick Ⅰ-Ⅱ 型)的人群,老年斑出现时间比深色皮肤者早 8-12 年,且面积更大;
- 机制:黑色素细胞可吸收部分紫外线,保护角质形成细胞免受 DNA 损伤,而白皙皮肤的黑色素含量低,防护能力弱,导致突变累积更快(《肤色与皮肤老化》)。
这与 “白种人老年斑发生率远高于黑种人” 的临床数据一致,印证了色素防护的作用。
四、代谢因素:年龄增长导致的 “清除能力下降”
老年斑的形成不仅是 “细胞增殖过多”,也与 “代谢清除不足” 相关,这一因素随年龄增长愈发显著:
1. 色素代谢减慢
老年斑中的黑色素并非 “合成过多”,而是 “清除减慢”:
- 随年龄增长,皮肤巨噬细胞的吞噬能力下降 40%,无法及时清除死亡细胞释放的色素颗粒;
- 这些颗粒在角质层堆积,使老年斑呈现 “棕黑色”,且颜色随年龄加深(《色素代谢与老化》)。
这解释了为何老年斑的颜色与紫外线暴露程度正相关 —— 紫外线刺激黑色素合成,而代谢减慢使其无法排出。
2. 抗氧化能力衰退
皮肤的内源性抗氧化系统(如谷胱甘肽、超氧化物歧化酶)在 60 岁后活性降低 50%:
- 抗氧化能力不足导致 ROS 在细胞内累积,加重 DNA 损伤;
- 临床数据:血清维生素 E 水平低的老年人,老年斑发生率比正常水平者高 60%(《抗氧化与皮肤健康》)。
五、特殊类型老年斑的诱因:与疾病的关联
少数老年斑的早发或快速增多可能提示潜在健康问题,其诱因具有特殊性:
1. 突然增多的老年斑:可能与内脏肿瘤相关
- 罕见情况下(<1%),短期内(6 个月内)出现大量老年斑(>50 个),可能是 “Leser-Trélat 征”,提示胃肠道或肺部恶性肿瘤;
- 机制:肿瘤分泌的生长因子(如转化生长因子 β)通过血液到达皮肤,刺激角质形成细胞异常增殖(《副肿瘤性皮肤病》)。
这种 “恶性老年斑” 的特点是:伴随瘙痒、快速增大,且多为扁平型(与普通老年斑的隆起型不同)。
2. 日光性角化病合并老年斑
长期户外工作者可能出现 “日光性角化病 - 老年斑” 混合病变,其诱因是:
- 紫外线导致的 DNA 损伤更严重,同时存在 p53 突变与染色体畸变,这类病变的恶变风险(进展为鳞癌)约 1%-3%,需积极治疗。
六、老年斑是 “遗传基础 + 紫外线损伤 + 代谢衰退” 的必然结果
老年斑的成因可概括为:遗传决定 “易感性”,紫外线提供 “损伤累积”,年龄增长导致 “修复与代谢能力下降”,三者共同促使角质形成细胞发生 p53 突变,出现异常增殖与色素沉积。
与其他色斑相比,老年斑的核心是 “细胞增殖失控” 而非单纯色素问题,这也是其更顽固、需医疗干预才能彻底去除的原因。理解这些成因有助于针对性预防 —— 年轻时严格防晒、增强抗氧化,可显著延缓老年斑的出现时间,降低严重程度。这一结论基于分子生物学与临床观察,为老年斑的预防和治疗提供了科学依据。
踩一下[0]

顶一下[0]